24-06-19
Амид относится к типу соединения, в котором ацильный углерод связан с амином. Функциональная группа может быть записана как R1C(=O)NR2R3, где R1, R2 и R3 могут быть атомами водорода или органическими группами. Амиды также можно рассматривать как органические соединения, образующиеся при конденсации карбоновой кислоты и аммиака или амина. К простым амидам относятся: формамид, ацетамид, бензамид и N,N-диметиламид.
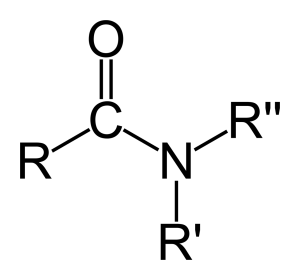
Общая формула амида
McLean предлагает различные типы амидных реагентов и их производных, которые обладают характеристиками высокой чистоты, передовыми технологиями производства и поддержкой индивидуальных исследований и разработок. Они могут широко использоваться в различных научно-исследовательских проектах и исследовательских экспериментах. Добро пожаловать к покупке.
В этой статье кратко представлены характеристики продукта и связанные с ним применения реагента Маклинамид по следующим пунктам:
1.Применение амида
2. Строение амида
3. Свойства амидов.
4.Синтез амидов
5. Реакция амидов
6. Знакомство с реагентом Маклинамид и сопутствующими продуктами.
Применение амидов
Амиды широко распространены в природе и имеют важное применение в науке и технике. Пептидные связи в белках соединены амидными структурами. Промышленно важные химические материалы, такие как нейлон, арамид, теворн и т. д., представляют собой синтетические волокна, полимеризованные из мономеров, содержащих амидные структуры. Многие лекарства также содержат амидные структуры, которые помогают поддерживать жесткую структуру и противостоять гидролизу, например ацетаминофен, пенициллин, ЛСД и т. д. Некоторые низкомолекулярные амиды обычно используются в качестве органических растворителей, таких как ДМФ и ДМАц.

Нейлон 66 синтезирован в лаборатории
Строение амида
Связь C-N в амиде короче связи C-N в амине. С одной стороны, это связано с тем, что углерод в связи C-N в амиде использует гибридные орбитали sp2 для связи с азотом, а углерод в связи C-N – с азотом. С другой стороны, амин использует гибридные sp3-орбитали для связи с азотом, поскольку неподеленная пара электронов на азоте делокализована на карбонильной группе, образуя сопряженную систему между углеродом, азотом и кислородом. так что связь CN имеет определенные свойства двойной связи. Следовательно, N, O и C в амиде находятся в одной плоскости, ограничивая вращение вокруг ацильной группы.
Шаровидная модель молекулы формамида, показывающая делокализацию π-электронов
Структура амида имеет следующую резонансную формулу:
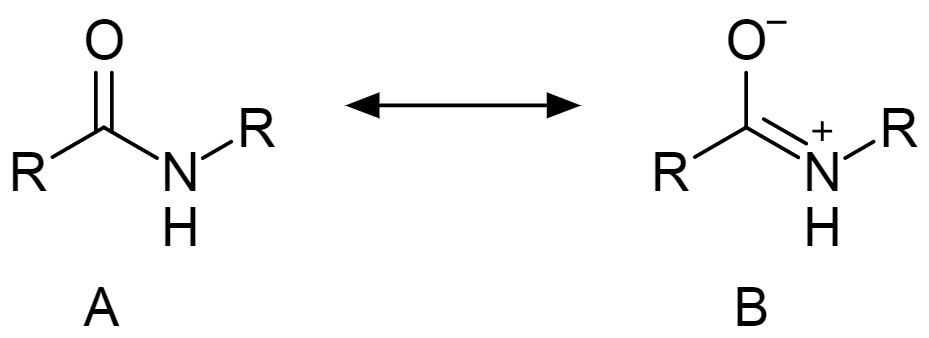
Свойства амидов
За исключением формамида, большинство амидов со структурой RCONH2 представляют собой твердые вещества белого цвета из-за образования водородных связей между молекулами. Среди производных карбоновых кислот амиды обладают наибольшей стабильностью и труднее всего гидролизуются, обычно требуя кипячения с обратным холодильником в сильнокислых или щелочных условиях. По сравнению с аминами амиды обладают более слабой щелочностью, а низшие амиды растворимы в воде. Например, ДМФ и ДМАц являются хорошими апротонными полярными растворителями и смешиваются с водой. Он может реагировать с кислотами с образованием солей, при этом его протонирование происходит по атому кислорода. Щелочность амидов слабее, чем у аминов, но сильнее, чем у сложных эфиров, кетонов и карбоновых кислот. Атомы водорода у имидов слабокислые.
Белки и пептиды являются важными биомолекулами, содержащими амидные связи. Некоторые алкалоиды также содержат амидные структуры.
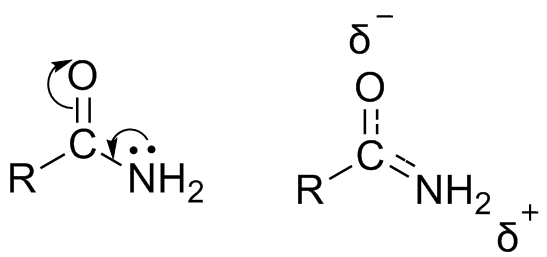
Синтез амидов
Амиды можно получить путем сочетания карбоновых кислот с аминами. Прямая реакция требует высоких температур для вытеснения воды из системы:
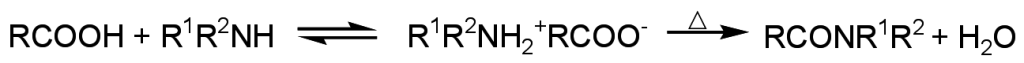
Сочетание карбоновой кислоты с амином для прямого синтеза амида
Амиды можно синтезировать путем взаимодействия сложных эфиров, ангидридов (метод Люмьера-Барбьера) или хлорангидридов (реакция Шонтена-Баумана) с аминами. При синтезе пептидов амиды синтезируются с помощью связующих агентов (таких как HATU, HOBt, PyBOP). Некоторые реагенты, такие как реагент амидирования Шеппарда, используются для создания амидных и иминных структур.
Другие реакции
Органическое соединение рутения катализирует дегидрогенативное ацилирование аминов. Альдегид, полученный дегидрированием спирта, реагирует с амином с образованием полуаминового альдегида, который затем дважды дегидрируется с получением амида. Побочным продуктом этой реакции является водород:

Реакция амида с амином с образованием нового амида называется реакцией амидного обмена. Эта реакция протекает очень медленно и требует катализа кислотой Льюиса и металлоорганического катализатора:
RC(O)NR’2 + HNR”2 → RC(O)NR”2 + HNR’2
Амидная реакция
Амиды реагируют аналогично сложным эфирам, но менее реакционноспособны, чем сложные эфиры. Амиды гидролизуются в условиях горячей щелочи или сильной кислоты. При кислотном гидролизе образуются соответствующие ионы карбоновой кислоты и аммония, а при щелочном гидролизе образуются соответствующие ионы амина и карбоксилата. Поскольку условия гидролиза амидов более интенсивны, чем у сложных эфиров и галогенангидридов, реакция не требует катализа и является необратимой.
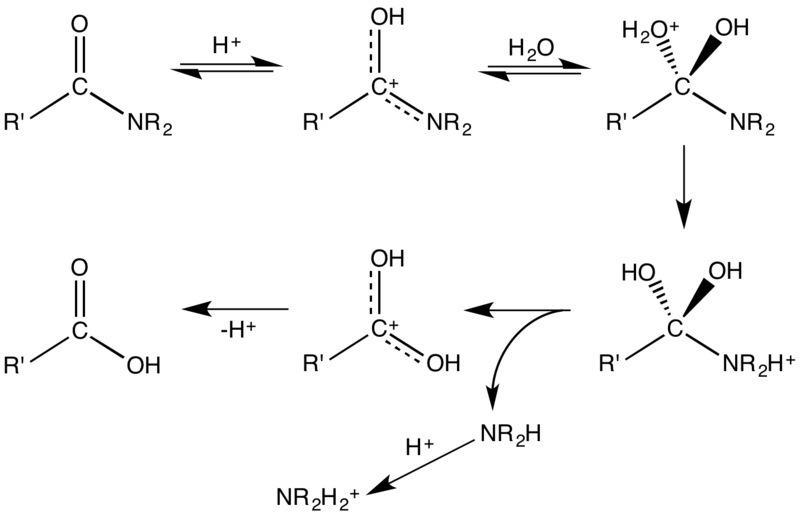
Механизм кислотного гидролиза амидов

Кислотный и щелочной гидролиз амидов.
| реакция | продукт | Условия реакции |
| обезвоживание | Нитрил | P2Os;бензолсульфонилхлорид; TFAA+py; |
| Перегруппировка Хаффмана | Первичные амины с одним атомом углерода меньше | Бром + гидроксид натрия |
| снижение | Амины и альдегиды | i) LAH ii) H+/H20 |
| Реакция Вильсмайера-Хаака | альдегид | POCI3, ароматический субстрат |
| Реакция Бишлера-Наперальского | Циклический имин | POCls, sOClz и т. д. |